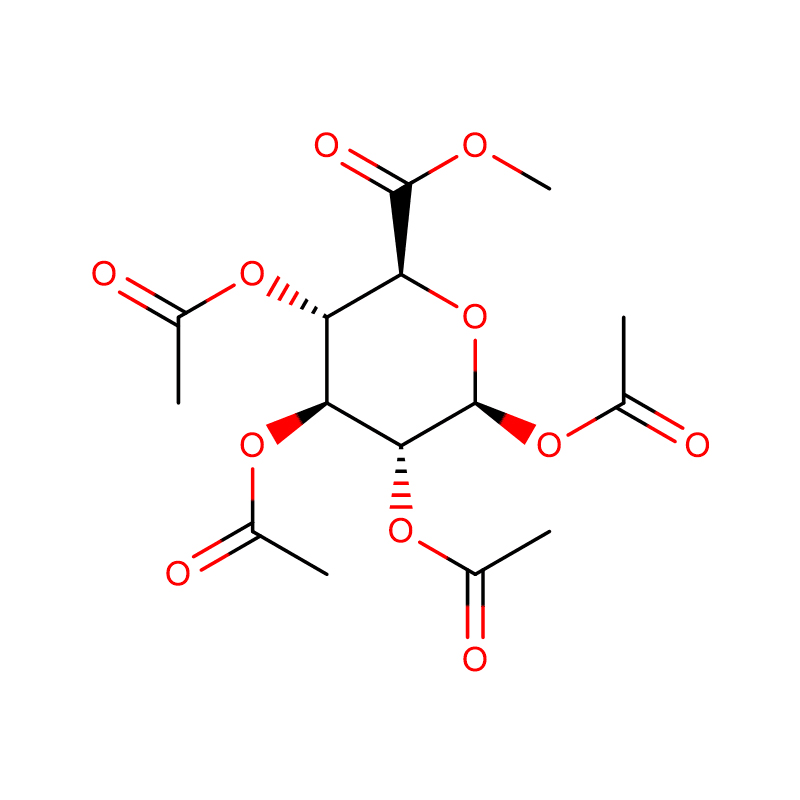
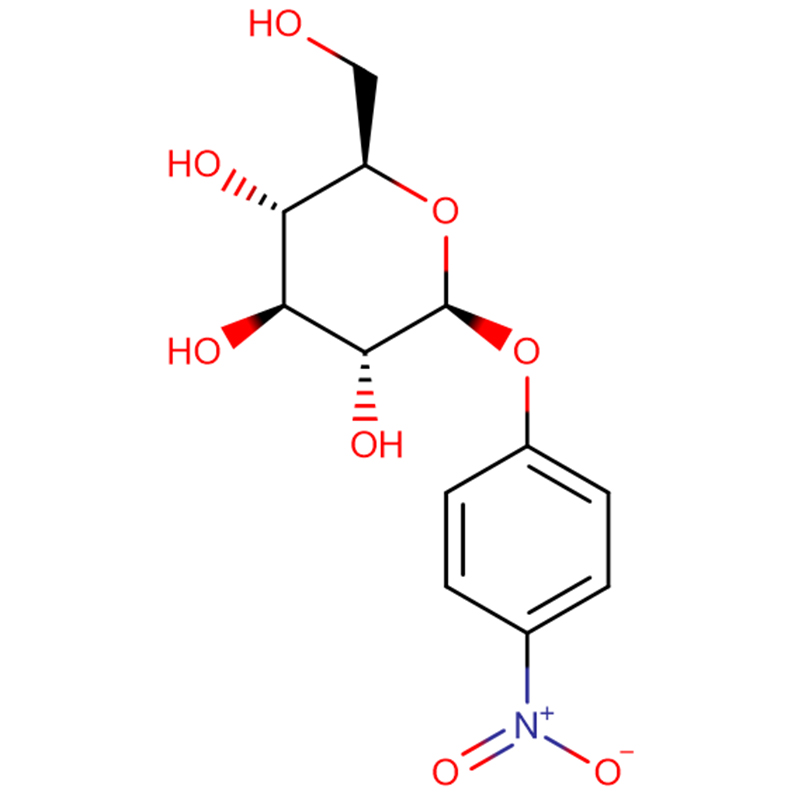
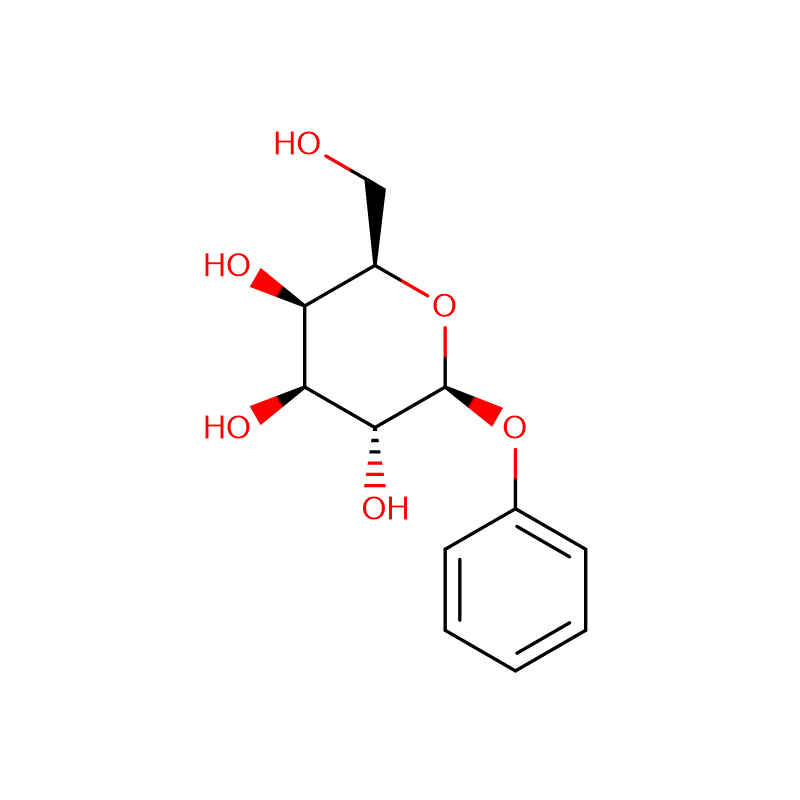
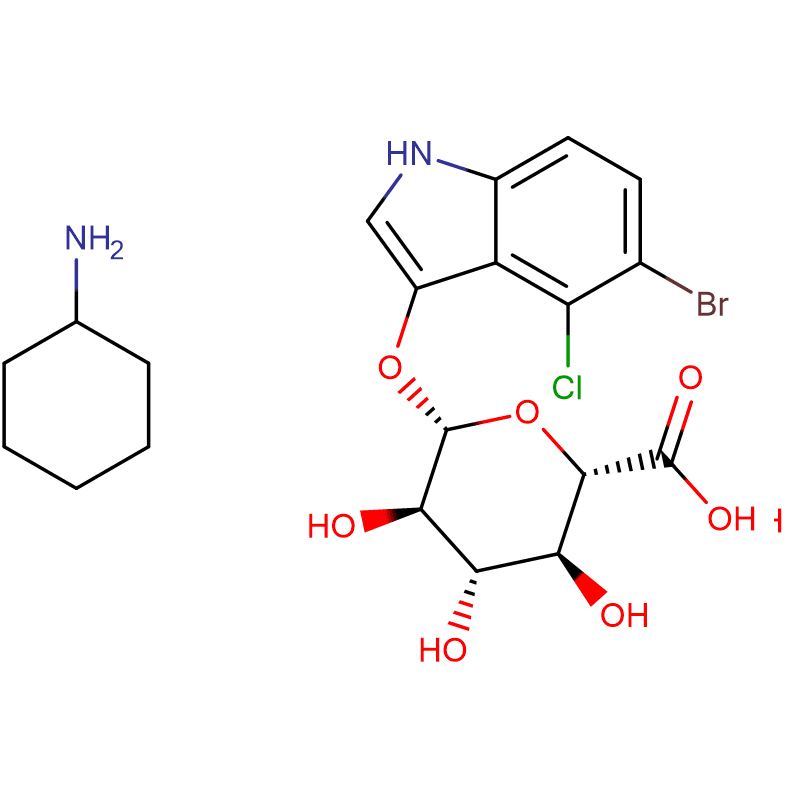
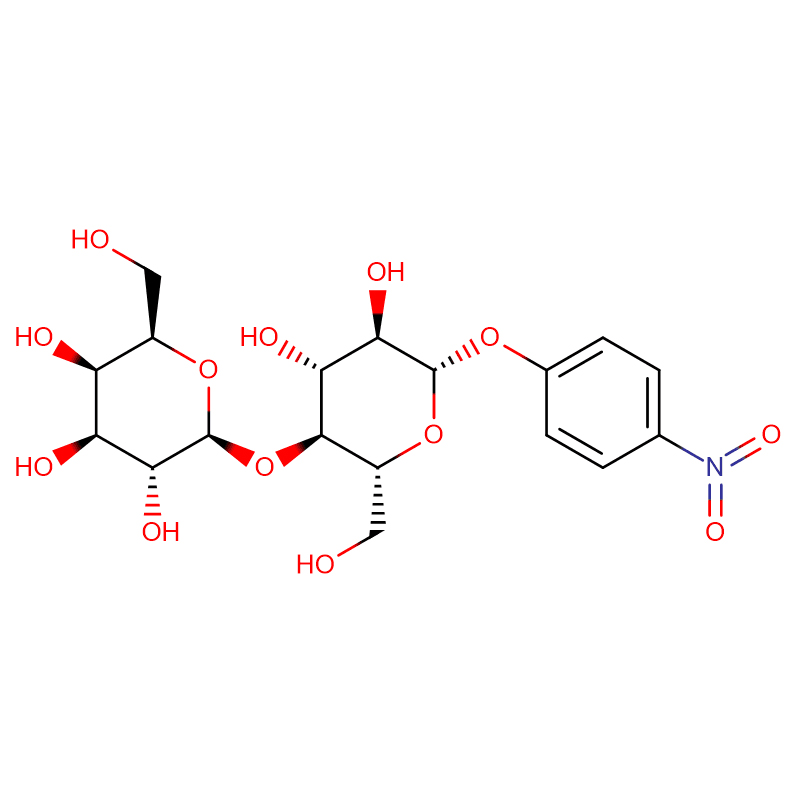
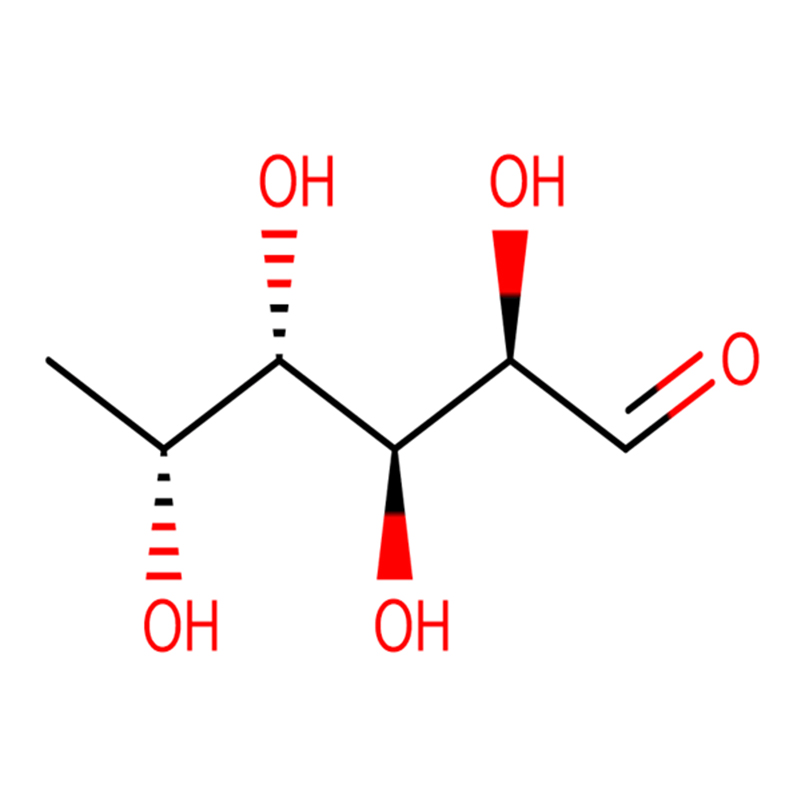
Два изомерных бицикло[4.1.0]гептановых аналога ингибитора гликозидазы галактовалидамина, (1R*,2S,3S,4S,5S,6S*)-5-амино-1-(гидроксиметил)бицикло[4.1.0]гептан -2,3,4-триол синтезировали в 13 стадий из 2,3,4,6-тетра-О-бензил-D-галактозы.Ингибирующую активность двух конформационно ограниченных аминов и соответствующих им ацетамидов измеряли в отношении коммерческих ферментов альфа-галактозидазы из кофейных зерен и E. coli.Активность фермента семейства гликозилгидролаз GH27 (кофейные зерна) конкурентно ингибировалась 1R,6S-амином (7), связывающее взаимодействие, которое характеризовалось значением K(i) 0,541 мкМ.Альфа-галактозидаза E. coli GH36 демонстрировала гораздо более слабое связывающее взаимодействие с 1R,6S-амином (IC(50)=80 мкМ).Диастереомерный 1S,6R-амин (9) слабо связывался с обеими галактозидазами (кофейные зерна, IC(50)=286 мкМ) и (E.coli, IC(50)=2,46 мМ).