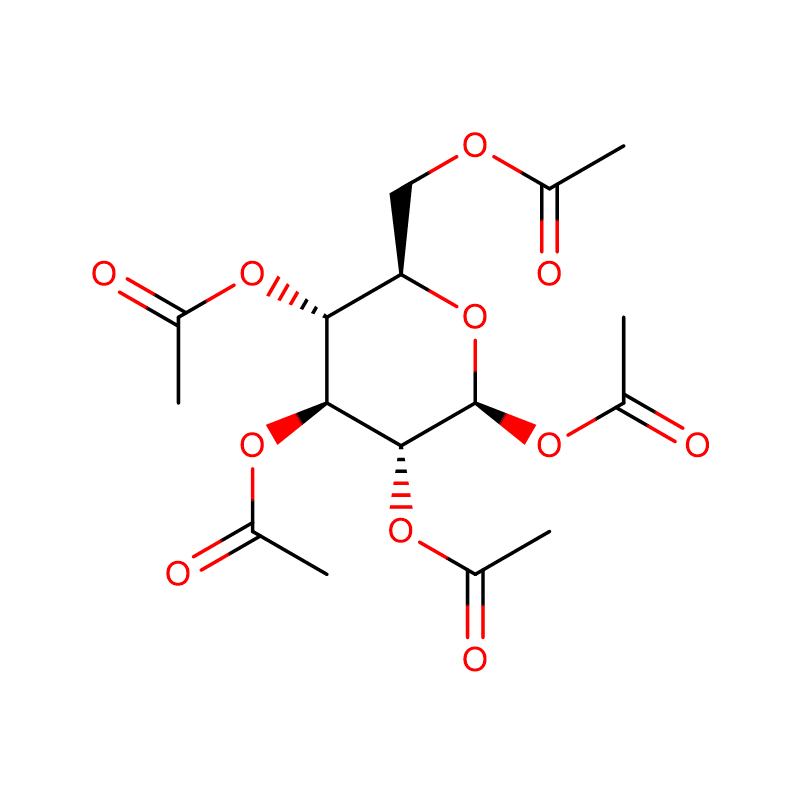
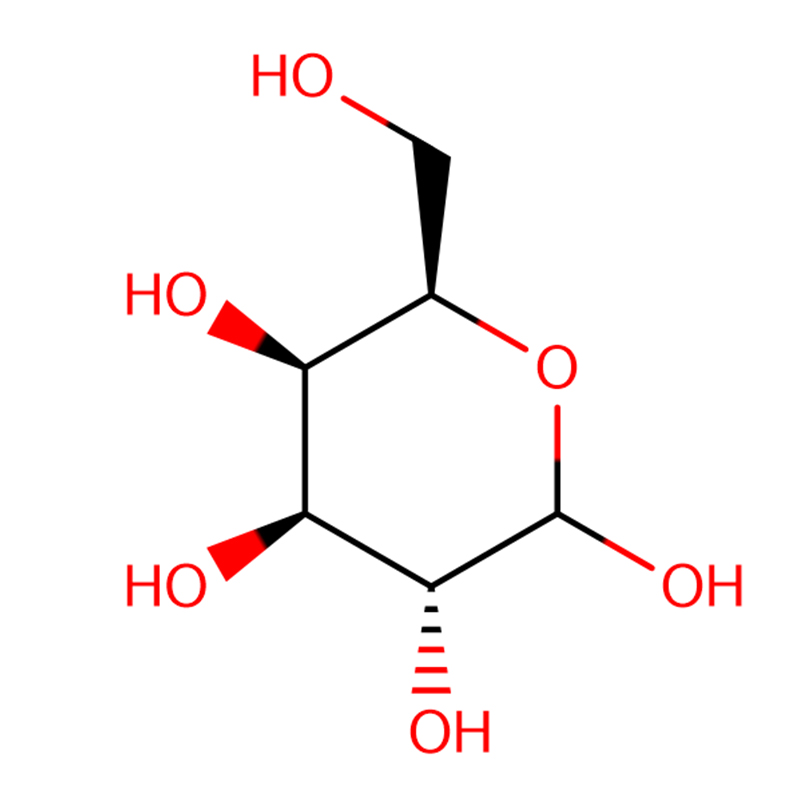
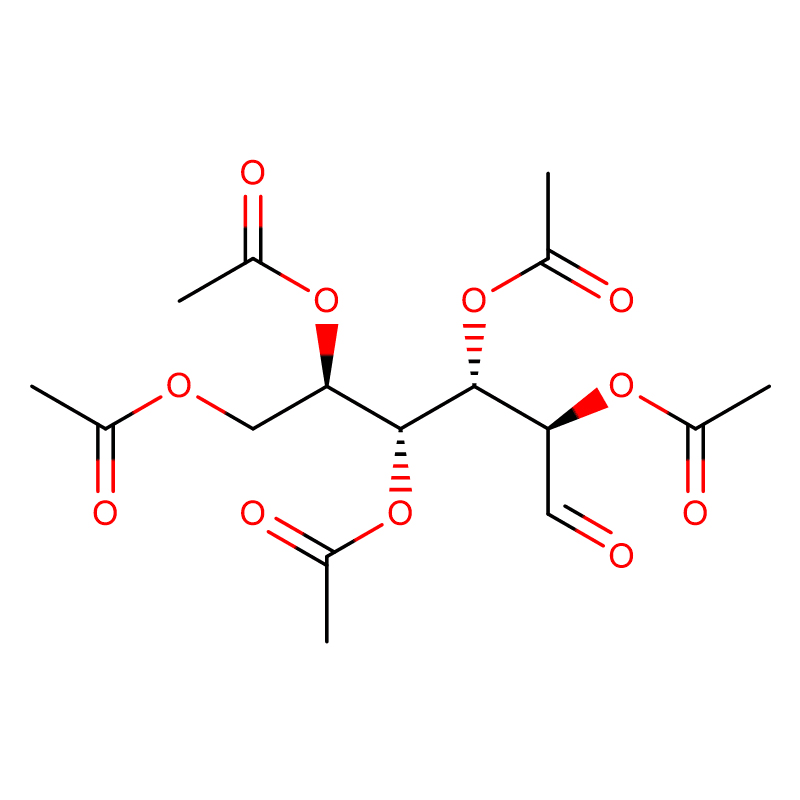
4-НИТРОФЕНИЛ-АЛЬФА-D-МАННОПИРАНОЗИД CAS:10357-27-4 Не совсем белый порошок 98%
| Номер каталога | XD90011 |
| наименование товара | 4-нитрофенил-альфа-D-маннопиранозид |
| КАС | 10357-27-4 |
| Молекулярная формула | C12H15NO8 |
| Молекулярная масса | 30301,25 |
| Сведения о хранилище | -2к -8°С |
| Гармонизированный тарифный кодекс | 29400000 |
Спецификации продукта
| Вода | <5% Карл Фише |
| Растворимость | 1% в ДМФА прозрачен и бесцветен. |
| Чистота | Свободный 4-нитрофенол <200 частей на миллион |
| ВЭЖХ | >98% |
| Появление | Не совсем белый порошок |
Механистическое понимание Са2+-зависимого семейства альфа-маннозидаз в кишечном симбионте человека.
Бактерии толстой кишки, примером которых являются Bacteroides thetaiotaomicron, играют ключевую роль в поддержании здоровья человека, используя большие семейства гликозидгидролаз (GH) для использования пищевых полисахаридов и гликанов хозяина в качестве питательных веществ.Такое расширение семейства GH иллюстрируется 23 гликозидазами семейства GH92, кодируемыми геномом B. thetaiotaomicron.Здесь мы показываем, что это альфа-маннозидазы, которые действуют через единый механизм замещения, чтобы использовать N-гликаны хозяина.Трехмерная структура двух маннозидаз GH92 определяет семейство двухдоменных белков, в которых каталитический центр расположен на границе домена, обеспечивая кислотную (глутамат) и основную (аспартат) помощь гидролизу в Ca(2+)- зависимый способ.Трехмерные структуры GH92 в комплексе с ингибиторами дают представление о специфичности, механизме и конформационном маршруте катализа.Ca(2+) играет ключевую каталитическую роль, помогая деформировать маннозид от его основного состояния (4)C(1) к переходному состоянию. (Библиография: Nat.хим.биол.6, 125-32, (2010)
Фронтальная аффинная хроматография гликоаспарагинов овальбумина на колонке с конканавалин-А-сефарозой.Количественное исследование специфичности связывания лектина.
Взаимодействия конканавалина А (КонА), иммобилизованного на сефарозе 4В, с 10 гликоаспарагинами, полученными из овальбумина, исследовали количественно с помощью фронтальной аффинной хроматографии.В этом методе углеводный раствор непрерывно подают в колонку с ConA-Sepharose и измеряют замедление фронта элюирования как параметр силы взаимодействия.Можно определить константу диссоциации (Kd) для каждого сахарида с ConA.Анализ связывания п-нитрофенил-альфа,D-маннозида показал, что связывающие свойства КонА существенно не изменяются после иммобилизации на сефарозе 4В.Каждый из гликоаспарагинов овальбумина был помечен тритием методом восстановительного метилирования для анализа.Сравнение полученных значений Kd показало, что связывание ConA значительно варьирует при очень незначительных структурных различиях гликозильной цепи.Результаты показывают, что ConA распознает специфическую структуру гликозильной цепи Man alpha 1-6(Man alpha 1-3)Man, в которой по крайней мере одна гидроксильная группа в положении C-3 маннозы, связанной с C-6, должна быть свободной.